
Хроническая сердечная недостаточность (ХСН) является одной из серьезных проблем во многих развитых странах мира. Это единственное заболевание сердечно-сосудистой системы, распространенность которого продолжает увеличиваться. Проблема распространенности ХСН чаще определяется возрастанием длительности жизни людей, то есть «старением» населения. Показатель выявляемости ХСН зависит от возраста пациентов и практически удваивается с каждым десятилетием жизни в возрасте после 45 лет. Серьезную не только медицинскую, но и социальную проблему представляет лечение пациентов с ХСН, требующее больших финансовых затрат.
Что такое сердечная недостаточность?
С патофизиологической точки зрения, сердечная недостаточность — это неспособность сердечной мышцы, при отсутствии снижения объема циркулирующей крови и уровня гемоглобина, обеспечивать кровью ткани в соответствии с их метаболическими потребностями в состоянии покоя и/или при умеренной физической нагрузке. Сердечная недостаточность — это патология, развивающаяся вследствие уменьшения способности миокарда сокращаться. При этом возникает несоответствие между предъявляемой к сердцу нагрузкой и возможностью сердца выполнять свою работу. ХСН развивается в результате нарушения обеих функции сердца: как систолической, так и диастолической.
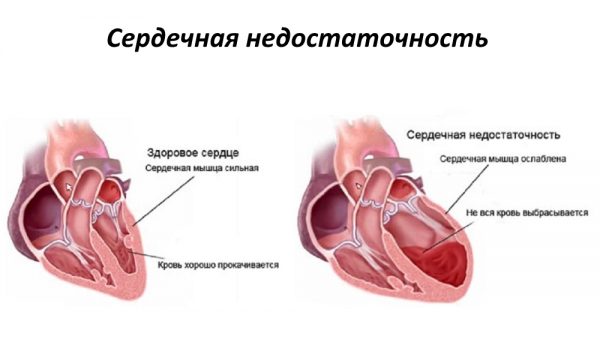
Систолическая функция — активный процесс, в результате которого мышца сердца сокращается, кровь выталкивается в сосуды и осуществляется перфузия внутренних органов и периферических тканей. Нарушение ударной функции, или систолическая сердечная недостаточность, является следствием ХСН независимо от причин, вызвавших развитие данного состояния. Традиционно ХСН связывают именно с систолической недостаточностью, которая в подавляющем большинстве случаев обусловливает развитие клинических симптомов, заставляющих пациента обратиться к врачу.
Не менее важное значение для нормального функционирования сердца имеет его диастолическая функция, то есть способность к расслаблению. Нарушение диастолической работы, или диастолическая сердечная недостаточность, в ряде случаев является основным при развитии и прогрессировании ХСН. При развитии диастолической недостаточности полости сердца обычно не расширены, миокард имеет нормальную сократимость, но нарушено наполнение желудочков кровью. Это снижение диастолического наполнения зависит как от изменения пассивной эластичности миокарда, так и изменения механизмов его активного расслабления. Ведущими факторами, определяющими изменения диастолического расслабления при ХСН, являются нарушения кальциевого обмена и энергетического обеспечения, изменение симпатической иннервации, процессы ремоделирования миокарда.
Практически при всех заболеваниях, приводящих к развитию ХСН, выявляются нарушения как той, так и другой функции сердца. Поэтому среди патофизиологических причин развития ХСН (как систолической, так и диастолической) можно выделить следующие.
Повреждение миокарда (миокардиальная недостаточность):
- 1. Первичные повреждения: физическое (травма миокарда, электротравма, радиоактивное облучение); химическое (токсическое действие нейрогормонов, лекарственных и нелекарственных агентов); биологическое (токсины, вирусы, паразиты и микроорганизмы); неуточненное и/или генетически детерминированное (кардиомиопатия).
- 2. Вторичные повреждения (ИБС, болезни эндокринной системы, соединительной ткани, наследственная миопатия, недостаток витаминов и ферментов и т. д.).
Повышенная гемодинамическая нагрузка на миокард в результате:
- перегрузки давлением (артериальная гипертензия, первично-сосудистая легочная гипертензия, стеноз устья аорты или легочной артерии );
- перегрузки объемом (недостаточность митрального, аортального или трехстворчатого клапанов, другие врожденные пороки сердца);
- комбинированной перегрузки.
Нарушения ЧСС (тахисистолические формы нарушения сердечного ритма, брадисистолия). Возрастные изменения.
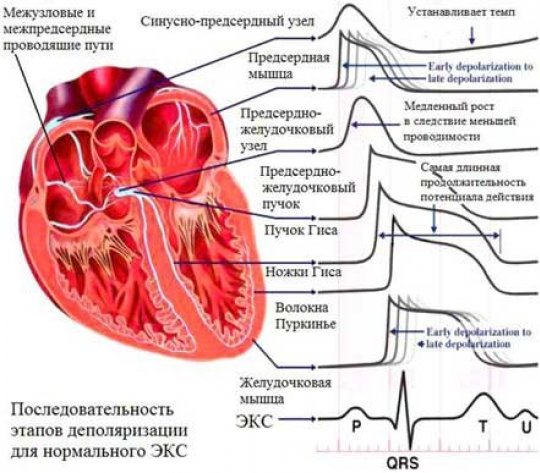
Экстракардиальные причины (сдавление сердца экссудатом или опухолью, изменения перикарда, тампонада сердца, нарушения функции эндокринных органов, при гипотиреозе, сахарном диабете и др.).
Несмотря на разнообразие причин, приводящих к формированию сердечной недостаточности, развитие ХСН проходит три основных этапа: начальный, адаптационный и конечный:
- 1. На начальном этапе происходит повреждение миокарда, либо сердце начинает испытывать повышенную гемодинамическую нагрузку, в результате чего развивается дисфункция миокарда, сущность которой заключается в несоответствии между сердечным выбросом и метаболическими потребностями органов и тканей. Следствием понижения сердечного выброса является уменьшение перфузии органов и тканей.
- 2. Для адаптационного этапа характерно привыкание организма к измененным условиям функционирования. Начальная стадия сердечной недостаточности протекает без существенных нарушений внутрисердечной и системной гемодинамики. Это происходит в результате включения механизмов адаптации. Механизмы адаптации, или компенсации, при ХСН охватывают все функциональные системы — от клеточного уровня до всего организма. Адаптационные механизмы ХСН включают изменения нейроэндокринной регуляции, альтернативные и заместительные пути метаболизма, кардиальные факторы — закон Франка-Старлинга, процессы ремоделирования как миокарда, так и его составляющих на клеточном и молекулярном уровнях.
- 3. На конечном этапе происходит формирование фенотипа ХСН. В результате реализации компенсаторно-адаптационных реакций на различных уровнях у многих больных функциональное состояние большинства систем организма до определенного времени остается практически нормальным. Но со временем поддерживающие механизмы преобразуются в патогенетические факторы. В результате «включения» несколько механизмов (длительная активация или гиперактивация нейрогуморальных систем, ремоделирование сердца и т. д.) происходит дальнейшее ухудшение функционирования миокарда и развиваются необратимые изменения в сердце, то есть формируется фенотип ХСН.
Сердечная недостаточность бывает острая и хроническая:
- Острая сердечная недостаточность возникает как следствие какой-либо катастрофы: тяжелые нарушения ритма сердца (пароксизмальная тахикардия, фибрилляция желудочков и другие), инфаркт миокарда, острый миокардит, острое ослабление сократительной функции миокарда у больных с пороками сердца, эмболия ствола легочной артерии.
- Хроническая развивается постепенно, в течение длительного времени. Причинами могут быть аортальный порок, митральная недостаточность, гипертоническая болезнь, эмфизема легких, пневмосклероз.
Различается сердечная недостаточность и по отделам сердца.
Выделяют компенсированную и декомпенсированную сердечную недостаточность:
- Компенсированная ХСН — это ранние, скрытые формы сердечной дисфункции, когда обменные потребности органов и тканей в фазу отдыха обеспечиваются при помощи активации компенсаторных механизмов.
- Декомпенсированная — это манифестные формы патологического состояния, когда заболевание проявляется рядом симптомов. Одышка в сочетании с признаками увеличения объема жидкости (отеки) или без них — самый распространенный клинический симптом сердечной недостаточности. Высокая степень одышки не соотносится со степенью вызвавшей ее дисфункции левого желудочка (ЛЖ ), которая является в большей мере значимым показателем прогноза.
Патофизиология сердечной недостаточности
Патофизиология ХСН считается тяжелым разносторонним процессом. ХСН представляет собой сочетание проявлений первичных патологических влияний и целого комплекса компенсаторных механизмов. Несмотря на то, что клиническая диагностика синдрома ХСН обычно не вызывает больших трудностей, тонкие патофизиологические и биохимические сдвиги, происходящие при этом, значительно труднее поддаются изучению. Учитывая первые концептуальные модели (кардиальной и кардиоренальной) патогенеза, основная причина в возникновении ХСН принадлежала снижению сократительной деятельности сердца, а также обмену электролитов и воды в организме. Широкое использование данной концепции повлекло за собой активное использование в клинике сердечных гликозидов, а затем и диуретических средств для лечения застойного синдрома.
В середине 70-х гг. XX века наиболее известной была кардиоциркуляторная модель. При возникновении нарушения функции миокарда формируются компенсаторные изменения гемодинамики, которые делятся на гетерометрические (увеличение преднагрузки, гипертрофия миокарда) и гомеометрические (увеличение частоты циклов сердечной деятельности, увеличение большого периферического сопротивления). Эти изменения гемоциркуляции, первично направленные на увеличение ударной величины и/или поддержание артериального давления при уменьшении сердечного выхода за счет механизмов Франка-Старлинга (повышение силы и скорости сокращения сердечной мышцы с увеличением длины волокна), Боудича (увеличение силы и скорости сокращений сердечной мышцы с увеличением частоты сердечного ритма), Анрепа (рост силы сокращения сердца при нарастании постнагрузки), потом начинают оказывать отрицательное действие, способствуя развитию декомпенсации сердечной деятельности.
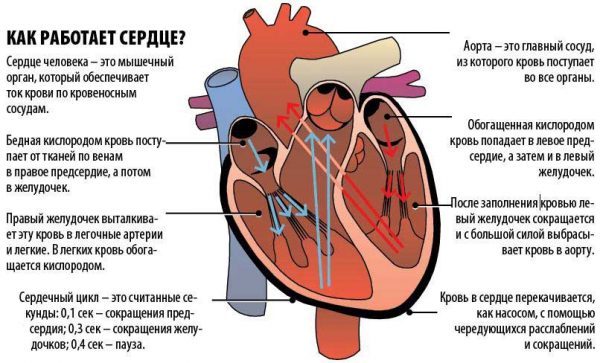
С гемодинамической точки зрения, сочетание понижения притягивающей функции миокарда и изменений периферического кровообращения, связанных с изменением пред- и посленагрузочных характеристик, считается главной причиной манифестации ХСН. Согласно этой идее, в практику лечения ХСН были введены препараты, влияющие как на центральную, так и на периферическую гемодинамику. Однако многочисленные клинические исследования привели к разочарованию в инотропных стимуляторах (симпатомиметики, ингибиторы фосфодиэстеразы) и далеко не однозначной оценке эффективности и безопасности вазодилататоров при снижении функции левого желудочка. Прогрессирование ХСН не столь близко связано с состоянием притягивающей функции сердца, как полагали раньше. Состояние притягивающей функции левого желудочка не имеет тесной сопряженности с толерантностью к физической нагрузке.
80-е — начало 90-х гг. охарактеризовались созданием нейрогормональной теории патогенеза ХСН. Нервногуморальная модель достаточно широко известна и согласована результатами многих испытаний, в которых продемонстрировано увеличение выживаемости пациентов с ХСН после нейрогуморальной разгрузки сердца с помощью блокаторов ангиотензинпревращающего фермента (ИАПФ). Хорошие результаты в применении ИАПФ ускорили поиск других нейрогуморальных стимуляторов для лечения больных с ХСН, активно изучается возможность применения непептидных антагонистов рецепторов к ангиотензину II I-го субтипа. Создание новых групп фармакологических препаратов для лечения ХСН близко связано с удачами патофизиологии и биохимии в рассмотрении роли нейрогуморальных изменений в патогенезе и саногенезе ХСН.
Перечень нейроэндокринных систем, активированных (на сосудистом и, что более важно, на местном уровне) при ХСН, является достаточно обширным. Среди наиболее изученных регуляторных систем, имеющих отношение к нейрогуморальной теории патогенеза ХСН, следует назвать ренинангиотензиновую, альдостероновую, симпатико-адреналовую, эндотелиновую, калликреин-кининовую, натрийуретическую, вазопрессиновую, адреномедуллиновую, нейроэндопептидазную. Данные, касающиеся новых групп медиаторов, которые активизированы при ХСН, представляют интерес не только с точки зрения патофизиологии, но имеют большое значение в совершенствовании терапии заболевания.
На этом программа по выделению патогенетических механизмов ХСН не прекратилась. Не так давно была представлена юная теория прогрессирования ХСН, базой которой является предположение об иммунной активации и системном воспалении как о знаках неблагоприятного прогноза и высокого сердечноваскулярного риска. По этой теории, неспецифический запуск макрофагов и моноцитов, работающий при сильных сдвигах микроциркуляции, является активатором создания провоспалительных цитокинов, ответственных за эволюцию дисфункции ЛЖ.
«Содействие» иммунной системы с патогенезом ХСН может показаться необычным. Но иммунная защита организма активируется не только при взаимодействии с инфекционными агентами, но также при нарушении поступления артериальной крови, гемодинамической перегрузке и иных влияниях на сердце, являющихся первоначальным звеном развития диастолической и/или ударной нарушенной функции.
Благодаря удачному развитию идей молекулярной биологии, способствующих исследованию в области генетики, в последнее время появились работы, посвященные изучению вклада генетических причин в развитие ХСН. Этому способствовало формирование теории «фенотипической модуляции», основывающейся на данных базовых исследований в таких науках, как генетика и клеточная биология. Фенотипическая модуляция подразумевает компетентность клеток изменять свой фенотип и функцию в пределах одной и той же ткани.
Нынешняя теория патогенеза ХСН сочетает в себе все написанные выше концепции на основе их взаимодополнения, так как не приходится опираться на то, что с помощью единой достаточно логичной теории патогенеза можно объяснить все нарушения у больного с сердечной недостаточностью и, тем более, решить все проблемы лечения, оказывая влияние на единственный механизм формирования и прогрессирования нехватки кровообращения.
Нейрогуморальная активация при ХСН
Изменение активности нейрогуморальных систем являет одним из ведущих адаптивных механизмов, направленных на поддержание сердечного выброса и уровня артериального давления, что необходимо для обеспечения нормальной перфузии тканей. В ряде случаев нейрогуморальная активация может служить фактором длительной адаптации. Однако нейрогуморальная активация в результате перманентного избыточного регуляторного ответа в итоге оказывает негативное влияние на деятельность сердечно-сосудистой системы и становится одним из ведущих патогенетических механизмов ХСН.
В процессе эволюции ХСН можно выделить три этапа нейрогуморальной активации:
- 1. Ухудшение функции миокарда ведет к уменьшению сердечного выхода и снижению артериального давления. Последнее за счет влияния на артериальные барорецепторы приводит к нарастанию эфферентной симпатической самоактивации, результатом которой являются быстрое повышение объема крови в полостях сердца и активация кардиопульмональных барорецепторов с целью уменьшить симпатическую активацию и увеличить выработку предсердного натрийуретического гормона. Повышение последнего направлено на снижение активации симпато-адреналовой системы (САС) и предотвращение повышения активности РААС.
- 2. Со временем блокирующее влияние сердечно-легочных барорецепторов на САС уменьшается, и симпатическая иннервация (в первую очередь сердца) увеличивается. Эфферентная почечная симпатическая иннервация приводит к активации РААС, чему на первых этапах противостоит система предсердного натрийуретического пептида. Однако его ингибирующее влияние достаточно быстро уменьшается, и активность РААС возрастает.
- 3. Активность САС и РААС значительно повышена, что приводит к дальнейшему снижению сердечного выброса и повышению реабсорбции натрия. Увеличивается чувствительность каротидных хеморецепторов, происходят обменные изменения в мышцах с запуском мышечных хеморецепторов даже при небольших физических упражнениях. Все эти изменения ведут к дальнейшему росту нейрогуморальной активности как циркулирующих, так и тканевых местных систем. Усиливается выработка различных эндогенных вазоактивных веществ, преимущественно вазоконстрикторного действия. Одновременно активируются процессы полиферации клеток, биосинтеза белка и образования коллагена (фиброза), то есть начинаются процессы ремоделирования сердца и сосудов.
Кардиальные компенсаторные механизмы
Основными кардиальными компенсаторными механизмами являются механизм Франка-Старлинга и ремоделирование миокарда.
Величина сокращения мышцы определяется ее длиной перед сокращением. С увеличением длины волокна происходит повышение силы сокращения и увеличение ударного объема. Этот механизм связан с тоногенной дилатацией желудочка сердца и относится к кардиальным факторам немедленной адаптации. Эффективность механизма Франка-Старлинга ощутимо уменьшается в условиях снижения сократимости миокарда и при значительном повышении диастолического давления в желудочках сердца. Повышение диастолического давления в желудочке выше определенного предела уже не приводит к увеличению длины мышечных волокон и дальнейшего усиления сердечного выброса не возникает.
Ремоделирование ЛЖ при сердечной недостаточности — это совокупность изменений его формы, величины внутреннего объема и веса миокарда, возникающих как ответ на неадекватные гемодинамические условия функционирования сердца или его повреждение. В клинически развернутой фазе систолической недостаточности ЛЖ феномен ремоделирования воплощается в его гипертрофии, дилатации и геометрической деформации.

Процесс нарастания гипертрофии сердечной мышцы представляет собой затянувшуюся адаптацию миокарда к увеличению гемодинамической нагрузки или локальному повреждению кардиомиоцитов. Развитие гипертрофии является компенсаторно-адаптационным механизмом, направленным, с одной стороны, на уменьшение внутримиокардиального напряжения благодаря утолщению стенок, а с другой — на сохранение возможности развивать достаточное внутрижелудочковое давление в систолу. Однако уже в самом процессе развития гипертрофии закладываются основы для дальнейшей декомпенсации миокарда.
Важнейшим фактором, который определяет развитие декомпенсации миокарда, является нарушение соотношения между сократительными элементами и капиллярной сетью и энергетический дисбаланс в гипертрофированном миокарде. При гипертрофии развитие капилляров значительно отстает от увеличения мышечных волокон. Отставание увеличения числа капилляров является одной из причин развития энергетического дефицита в гипертрофированном миокарде.
Развитие дилатации полостей является вторым конечным механизмом ремоделирования сердца. Увеличение полостей и изменена их геометрии позволяет на определенном этапе поддерживать более или менее адекватный сердечный выброс. Это достигается в результате возрастания объема крови внутри сердца. Сердце за счет увеличения остаточного объема способно выталкивать большее количество крови при значительно меньшей амплитуде сокращения. Однако формирование дилатации обычно происходит уже в условиях значительной поломки энергетического обмена в сердечной мышце, и дальнейшее увеличение полостей сердца сопровождается возрастанием внутримиокардиального напряжения и усилением активации тканевых нейрогуморальных систем, что быстро приводит к истощению энергетических резервов миокарда.
Декомпенсация
Длительное нарушение деятельности сердечно-сосудистого аппарата в итоге приводит к срыву компенсаторных механизмов и проявлению симптомов декомпенсированной сердечной недостаточности. Непосредственной причиной нарастания клиники ХСН могут быть разные моменты, многие из которых самостоятельно обычно не ведут к ХСН. Врач чаще всего может встретить следующую ситуацию: легочная эмболия, инфаркт миокарда, инфекция, анемия, тиреотоксикоз, беременность, нарушения ритма сердца (даже типичное возрастание частоты сердечных сокращений), воспаление сердечной мышцы, эндокарда, полиорганная гипертензия, тяжелые физические, эмоциональные, нутритивные и другие (в том числе медикаментозные) внешние стрессы.

Важно отметить, что прогноз у пациентов с сердечной недостаточностью, начальный механизм которой известен и убирается каким-либо образом (включая интенсивное лечение), более хорош, чем у пациентов, у которых основную причину узнать не удалось.
Несмотря на достигнутые успехи в лечении сердечной недостаточности, прогноз у таких больных остается неблагоприятным.
Видео Фото






